- 封面故事
- 2019年
- 600期-諾貝爾獎特別報導(12月號)
文章專區
2019-11-292019 諾貝爾化學獎 改變電器使用生態的鋰離子電池
600 期
Author 作者
顏宏儒/中研院化學所助研究員,致力於奈米石墨烯和鋰離子電池相關研究。

古迪納夫(John B. Goodenough, 1922~) 國籍|美國
任職單位|德州大學奧斯汀分校 機械工程和材料科學教授
研究領域|物理學
(Cockrell School of Engineering, The University of Texas at Austin)

吉野彰(よしの あきら, 1948~)
國籍|日本
任職單位|旭化成(株)吉野研究室室長
研究領域|電化學
(Asahi Kasei)
萬千選擇中,為何非「鋰」離子莫屬?
鋰原子的平均原子量只有 6.94,是最輕的金屬。此外,鋰的原子序是 3,意即它帶有三顆電子;在電子排列時,鋰的第三顆電子落在最外層,相當容易被釋放出來,也就是說,鋰具有很大的驅動力把電子傳給別的原子,活性相當大(圖一)。
在人類追求高電容量、輕量化的儲能設備時,鋰離子電池是能夠符合需求的選擇之一。與車用的鉛蓄電池相比,在提供相同的能量下,它可以絕對地輕量,並達到無線化及無石化燃料社會的可能性。
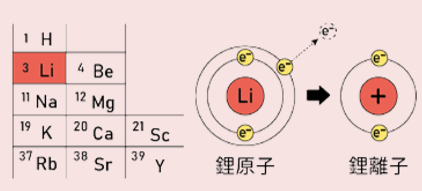
圖一:鋰最外層的電子易被釋出,並形成鋰離子。
一切電池的源頭──伏打電池
現今大家常用的電池,其實和最早發展出來的電池相當不同。最早的電池開發於18世紀,義大利科學家伽伐尼(Luigi Galvani)將兩種不同的金屬連接,然後同時觸碰青蛙腿的兩處神經,意外產生火花且造成蛙腿抽搐,他因此提出「動物電」的理論。
在這之後,另一位義大利科學家伏打(Alessandro Volta)則很快地也重複此實驗,認為應該不是動物電,伏打更意識到青蛙的腿是電的導體(即現今所說的電解質),便把青蛙的腿換成泡過鹽水的紙。後來他將鋅板和銅板交錯疊在一起,並在中間放了浸泡過鹽水的濕抹布,發現可以導電,進而開發出人類歷史上第一顆電池──伏打電池 (voltaic pile)。
伏打電池運作的原理主要是因為兩種金屬的活性不同,所發生氧化還原的現象:鋅的活性比較大,較容易把電子丟掉而發生氧化反應(負極),被丟掉的電子沿著外面的電路傳到銅片上產生還原反應(陰極),因為電子流動了所以可以導電。而濕抹布的角色被稱為「電解質」,負責傳導溶液中的離子,裡面的陽離子會在銅片這端得到電子而還原被析出,待陽離子全部析出後電池的壽命也就結束,此原理被持續使用至今天的一次性電池,也就是碳鋅電池和鹼性電池。
充電新生活革命: 關於鋰離子電池
人類在1970年代時意識到石油資源 有限,不可能無止境的開發,所以開始尋求其它如太陽能、風能等再生能源的開發,希望為人類找到除了化石燃料外的替代能源。而通常再生能源都是無法連續的,必須設法將這些能源儲存下來。
當時艾克森(Exxon)石油公司投入了新能源的研究,惠廷翰就是在那時加入艾克森並致力於開發最終能擺脫化石燃料的能源技術,成功發展出二硫化鈦(titanium disulphide), 製成能夠將離子嵌入的超導體,作為電池的陰極(圖二),並使用鋰金屬作為電池陽極,利用鋰的強大動力釋放電子,讓電子在陰陽極間流動,製備出的電池只有銀幣般的大小,已可提供太陽能手錶使用所需的電力。
.JPG)
圖二:以金屬鋰作陽極、嵌入離子的二硫化鈦作陰極的電池。
但當他試圖想要提升電池的工作電壓或製作更大型的電池時,電池經常著火。雖然因鋰的活性太大、易爆炸而無法使用,但仍開發出首個具有充放電功能的鋰離子電池,為往後鋰離子電池的發展奠定基礎。……【更多內容請閱讀科學月刊第600期】