- 科技報導
文章專區
2022-05-15「上帝的手術刀」誰有權操刀?由CRISPR專利糾葛 看生醫申請案的布局策略
485 期
Author 作者
許文馨/恆融智慧財產事務所專利師。
CRISPR源起
CRISPR,全名為「常間回文重複序列叢集」(clustered, regularly interspaced, short palindromic repeats, CRISPR),是一種源自於細菌的免疫系統序列,能夠記憶曾經來犯的病毒資訊,因此可以辨認並消滅相同的病毒。Cas9(CRISPR-associated protein 9)則是一種酵素,而由CRISPR與Cas9組成的系統作為CRISPR-Cas9基因編輯技術,可被用於精準地切割基因物質,進而編輯生物體內的基因,而被稱為「基因剪刀」。CRISPR-Cas9基因編輯技術具有快速、精準與跨物種的特性,能夠應用於生物醫學的相關領域中,特別是此技術有望根治基因突變引發的疾病,因此還有「上帝的手術刀」的盛譽。
夏彭提耶(Emmanuelle Charpentier)與道納(Jennifer Doudna)二位學者在2012年6月,首先將CRISPR-Cas9基因編輯技術的研究成果發表於期刊,而後這項技術也令她們獲得了2020年諾貝爾化學獎桂冠。除了夏彭提耶與道納的跨國研究團隊(以下簡稱道納團隊)外,美國哈佛大學與麻省理工學院共同創立的博德研究所(Broad Institute of MIT and Harvard)的張鋒團隊,也在2013年10月,將CRISPR應用於哺乳類動物細胞的突破性成果發表《科學》(Science)期刊,一併拉開了美國東西兩岸學術重鎮對這項技術爭霸戰的序幕。當然,除了在學術上爭奪榮耀與領先地位,二個團隊之間的專利戰火也不斷延燒。
(123RF)
基因剪刀剪不斷理還亂的專利爭議
在專利戰的戰場上,爭執核心在於雙方取得CRISPR技術專利申請日的時間點。道納團隊首先在2013年3月15日提出有關CRISPR的第一個專利申請案(第13/842,859號專利申請案,下稱859號案),該案主張2012年5月25日臨時申請案(Provisional Patent Application, PPA)的優先權,最初的範圍意欲不對該技術所適用細胞環境(cellular environment)進行限制。而張鋒團隊則是在2013年10月15日提出「CRISPR在哺乳類動物等『真核細胞』(eukaryotic cell)環境中編輯基因」的申請案(第14/054,414號專利申請案,下稱414號案),該案主張2012年12月12日臨時申請案的優先權。
在審查過程中,張鋒團隊申請加速審查(accelerated examination, AE)程序,所以他的申請案在2014年4月15日取得專利權。另一邊道納團隊則因為申請案的程序問題以及因所請範圍較廣,而不斷受到第三人對可專利性的挑戰,於2019年4月23日才獲准專利。在這期間,道納團隊於2016年向美國專利商標局(United States Patent and Trademark Office, USPTO)的專利審理暨訴願委員會(Patent Trial and Appeal Board, PTAB)申請專利衝突(interference)程序,主張雙方的專利申請案具有相同或是實質上相同的發明範圍,要求撤回張鋒團隊的專利權。
就專利衝突程序一役而言,在2017年2月的初步結果中,PTAB認為張鋒團隊的應用於真核細胞的CRISPR技術,與道納團隊的基因編輯技術屬於不同的發明,因此,雙方在CRISPR技術上並不重疊與衝突,所以判定張鋒團隊能保留其專利並擁有專利權。後續道納團隊上訴至聯邦法院,聯邦法院認同PTAB的裁決。
此後道納團隊再次出招,他們於2018年利用美國延續案(continuation application, CA)申請制度,提出了包含美國第15/947,680號專利申請案等14個延續案,試圖針對截至當時由張鋒團隊掌握專利權的CRISPR在真核生物細胞環境中編輯基因的範圍,取得專利權保護。據此,針對道納團隊此系列CA案與張鋒團隊的專利案與申請案,PTAB再次開啟衝突程序(第106,115號案)以確認該關鍵權利範圍究竟屬於何者。2022年2月28日,PTAB再次將「以CRISPR在真核生物細胞環境中編輯基因」的相關權利掌控權判給了張鋒團隊。
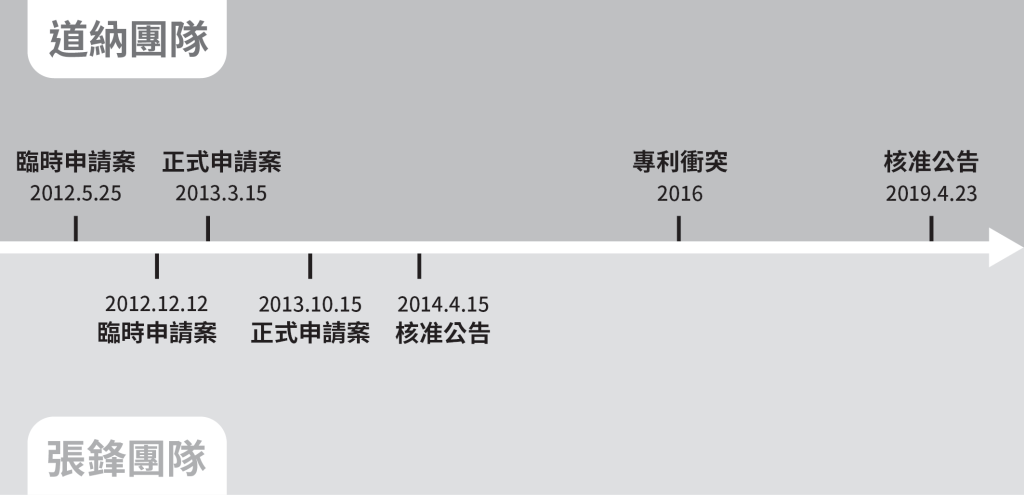
道納團隊與張鋒團隊的專利申請案歷程示意圖
在此次判決中,主要爭點在於究竟是哪個團隊實際將「CRISPR-Cas9系統用於編輯DNA,以影響真核細胞的基因表現」的概念付諸實現(reduced to practice)?在審視證據後,PTAB認為,張鋒團隊在2012年10月5日已將「成功在真核細胞中使用嵌合RNA的CRISPR-Cas9系統剪輯DNA」的論文草稿投稿於期刊;而道納團隊雖有可能在2012年10月5日前已在斑馬魚胚胎中進行DNA編輯,但沒有足夠證據證明該實驗是成功的,因此,後者沒有達到「付諸實行」的標準。除此之外,PTAB認為,道納團隊無法證實在2012年6月時對上述技術具有明確且永久(definitive and permanent)的想法。
雖然此案仍有上訴的可能,然而到目前為止,二個團隊各自握有專利權,但基於雙方對於申請專利範圍的解讀,即使現在道納團隊握有將CRISPR技術用於所有類型細胞和非細胞環境的專利權範圍,但未來若道納團隊與第三方希望將CRISPR技術實施於真核細胞環境中,仍需取得張鋒團隊的同意或授權。換句話說,在這樣的專利領土畫分之下,從今以後若第三方想要實施CRISPR技術,可能必須向雙方都取得授權才能進行。
從雙方專利布局看申請策略
回頭看二個團隊的審查歷程,很顯然地,無論是以主張優先權的臨時申請案申請日,還是正式申請案的申請日,張鋒團隊的414號案都晚於道納團隊的859號案,然而透過加速審查程序,414號案僅在6個月內就取得專利權,率先鞏固了張鋒團隊對於CRISPR於真核細胞中基因編輯的疆域。另一方面,道納團隊在提出申請後就被USPTO挑出與權利歸屬有關的形式問題(formalities issue),於2014年3月6日申請案公開後,又遭遇多次第三方意見(Third-Party Submission Under37 CFR 1.290)挑戰其可專利性──這些可能是導致859號案遲至2019年才獲准的部分原因。
然而,除了414號案與859號案之外,雙方在CRISPR技術相關領域的專利布局都不容小覷。事實上,道納團隊與張鋒團隊在專利布局策略上皆是步步為營,且各自利用臨時申請案、優先權、連續申請案的制度創造出交織的專利網絡,再配合加速審查制度,爭取盡速獲得完整的權利保護範圍。
臨時申請案的運用與權利範圍的規劃
由二個團隊專利申請的布局來看,雙方的申請策略都是利用臨時申請案取得優先權日,再於一年之內提出正式的專利申請案。因此,在主張相同母案作為優先權案的系列案中,各個子案都有它的技術相關性及延續性。在美國專利申請中,除了前述道納團隊應用的延續申請案,子案的態樣還包括部分延續申請案(continuation-in-part application, CIP)與分割案(division application, DA)。通過這些申請態樣,申請人可以藉由子案逐步擴張原有保護範圍,通過層層的網絡連結,將專利布局的範圍逐漸拓展,推得更深(技術延續性)及/或更廣(技術多樣性)。
就美國臨時申請案而言,由於它的揭露內容攸關後續作為優先權案的正式申請案的有效申請日,所以如何在臨時申請案中,揭露足夠的技術資料至關重要。也就是說,臨時申請案須滿足書面揭露要件(written description)才能作為正式案有效的優先權基礎。除此之外,臨時申請案轉為正式申請案時,正式申請案如何畫分欲請求的權利範圍也是一門學問。從以上道納團隊的申請策略來看,由於畫定的權利範圍較廣,即,不限制CRISPR技術的應用環境,可能導致後續排山倒海而來的第三方意見的攻擊與阻礙。另一方面,張鋒團隊將他主張的權利保護範圍限制於真核細胞環境,進而快狠準地取得保護範圍。因此,申請案的保護範圍規畫無疑是專利布局時至關重要的議題之一。
CRISPR案在產業面的影響
CRISPR技術在美國的專利之爭,因涉及數百萬美元的權利金而備受矚目。雖然PTAB在今(2022)年給出了最新的審查結果,此技術的相關專利爭議仍持續延燒。另外,由於CRISPR技術對於生技產業應用的範圍甚廣,此爭議不只在美國,而是在世界各地都熱烈延燒。在其它國家或區域如歐洲,相關議題甚至得到了不同的裁決結果,且除了道納團隊與張鋒團隊外,其它方亦加入戰局對關鍵性的CRISPR-Cas9專利權進行爭奪。
就美國戰場而言,張鋒團隊所屬的博德研究所事實上已發表聲明,希望能與道納團隊達成共識。博德研究所聲明指出:「複雜的專利與授權現況會威脅技術創新,而對於整個領域最好的發展,應是各方對解決方案達成共識,讓研究領域能聚焦於使用CRISPR技術解決現今實際上的問題。」
在今年2月PTAB的最新結果出爐後,博德研究所再次重申:「所有機構應該互相合作,以確保此具變革性的技術能廣泛且公開被取得,並持續探索最佳方法,以達到此目的。」
今年最新判決結果出爐後,若道納團隊與張鋒團隊仍執意就此議題再進行交鋒,欲實施CRISPR相關技術的第三方,可能需要同時向雙方尋求專利授權,如此一來,營運成本勢必大幅增加。較好的情形是,若道納團隊與張鋒團隊達成協議,則有可能通過交互授權或者是專利池(patent pool)的方式進行統一授權,對於第三方而言不失為一個解決方案。
除此之外,第三方亦可以通過採用不同的CRISPR系統,來避開道納團隊與張鋒團隊的專利技術範圍。舉例而言,可以採用Cas13或Cas14作為替代的酵素來執行CRISPR,這些酵素相當小且易於傳輸至人體細胞中,不失為一個解方。然而,需要注意的是,這些不同的酵素系統可能已由其它申請人的專利申請案或是專利公告案所涵蓋,因此在實施相關技術前,仍須尋求權利人的同意與授權。
結語
CRISPR-Cas9系統,原為科學研究的強大工具,已被運用在臨床疾病治療上,並進入人體試驗階段,未來的應用與發展潛藏無限商機。因此,CRISPR技術將如何發展,無疑是學界與業界矚目的話題。在美國東西岸兩強的專利戰之下,欲實施相關技術的企業必然面臨專利授權與技術轉移等現實層面的議題。另一方面,對於企業、政府的研發單位而言,在進行生醫領域的專利布局與策略規畫時,不妨借鏡CRISPR技術二大龍頭的布局方案,妥善且彈性利用各國專利申請制度,藉此提升專利布局的強度,進而獲致對自身技術更全面且有效的權利保護。
延伸閱讀
1. 王惠瑜,探討基因編輯技術CRISPR專利布局—以Jennifer Doudna與張鋒專利為例,科技政策觀點,https://portal.stpi.narl.org.tw/index/article/10345,2017月11月14日。
2. 李秉燊,CRISPR專利在美爭訟緣起、最新裁決與競合趨勢,北美智權報,2022年3月23日。
3. Heidi Ledford, Major CRISPR patent decision won’t end tangled dispute,Nature, 2022/3/9.