- 精選文章
文章專區
2018-11-01找尋細胞中的遺珠─遺失蛋白質
587 期
Author 作者
黃斌/高雄醫學大學生物醫學暨環境生物學系主任、幹細胞中心副主任,專長為一氧化氮及粒線體移植。
從人類於1953年確認去氧核醣核酸(deoxyribonucleic acid, DNA) 的雙股螺旋結構後約莫50年,就屬人類基因組計畫(human genome project, HGP)最具劃時代意義。為此,1988年國際人類基因組組織(The Human Genome Organization, HUGO)組織成立,以整合此跨國性大計畫。時至今日,幾乎各大物種的全基因序列皆已解碼完成。不過有趣的是,科學家似乎早就預知基因解碼必然成功,而真正的挑戰是在於後端的蛋白質鑑定與功能分析,因此 2001年,在人類蛋白體組織(Human Proteome Organization, HUPO)的架構下,開始執行人類蛋白體計畫 (human proteome project, HPP)。
什麼是遺失蛋白質?
此計畫中有2大分項研究,分別是「以染色體為主的人類蛋白質組計劃(chromosome-based Human Proteome Project, C-HPP)」及「生物與疾病的人類蛋白體計劃(Biology∕Disease Human Proteome Project, B∕D-HPP)」。其中,C-HPP的主要任務是分析基因表現與蛋白質表現的對應關係。截至目前為止,在人類蛋白質資料庫(neXtProt)的比對分析中,認為人類基因組可以轉譯(translation)出來的蛋白質有20159個。而在這些蛋白質中,不論是藉由質譜儀或抗體,已有17008個被證實其存在。另外,約有1939個只有透過基因轉錄(transcription)出的信使RNA(messenger RNA, mRNA)所逆轉錄(reverse transcription)的互補 DNA(complementary DNA, cDNA),卻無蛋白質存在的證據;有 563個蛋白質則界定為同源或非同源性蛋白質,亦即這些蛋白質序列太相近,以至於可能誤判為同一個蛋白質進而造成實際與預測的數量估算有所差異;還有77個蛋白質屬於生物資訊軟體預測應該為蛋白質,卻無基因轉錄與蛋白質轉譯的證據。因此,加總這三類群,共有2579個仍無法用質譜儀或抗體證明其表現,則統稱為「遺失蛋白質(missing proteins,圖一)」。 目前,隨著各國的進展,被鑑定到的遺失蛋白質數量亦不斷更新。
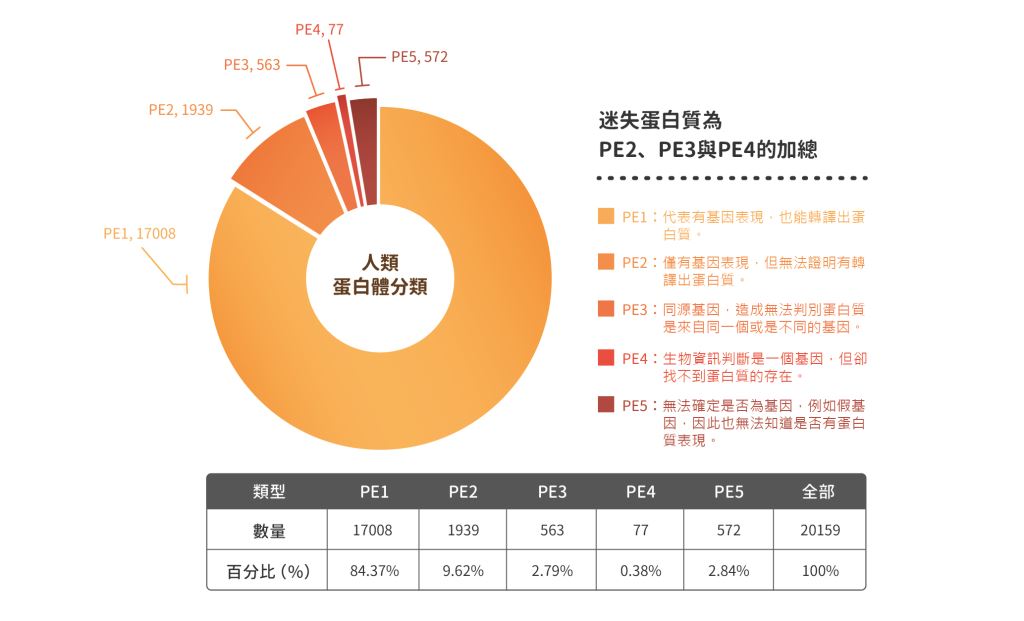
圖一:人類蛋白體分類,人類蛋白體組織中的資料庫將蛋白質證據(protein evidence)分成5 級。(人類蛋白體組織)
臺灣的遺失蛋白質計畫
遺失蛋白質的鑑定工作除了22+X+Y 共 24條染色體外,亦包含粒線體的基因組。不同於當初的基因解碼,在人類蛋白體組織中,臺灣正式被指定負責第四號染色體上的遺失蛋白質鑑定工作(圖二),而負責該項計畫的臺灣代表為中央研究院化學研究所陳玉如所長。筆者在一個偶然機會的會議中,與來自中研院、國衛院、臺大、陽明、成大、北醫、長庚及高醫的學者於會中討論遺失蛋白質計畫。所以,在經過腦力激盪後,分別針對生物資訊學再演算遺失蛋白質是否存在、重新鑑定質譜儀的分析數據、 根據互補DNA資訊合成遺失蛋白質抗體、從各種疾病重新找尋遺失蛋白質等各方向出發,正式進行該研究任務。2015 年,臺灣團隊發表利用同位素標定方式,進行更精準的質譜儀分析遺失蛋白質的存在。而在2017年的文獻中,高雄醫學大學則首度發表遺失蛋白質與肝癌形成的相關性,此亦為遺失蛋白質的表現與疾病的生理相關性被首度證實。

圖二:臺灣在臺灣蛋白體學會(Taiwan Proteoimcs Society, TPS)的與會下,正式取得第四號染色體遺失蛋白質之研究工作。不過,從臺灣開始進行遺失蛋白質研究到第一篇的論文發表,過程卻花了 5~6 年的時間。因此,這中間的困難該如何突破,就成了這群科學家一直思考的問題。而再將時光退回到 2000年,人類基因圖譜草稿公布時, 大家是否會有個疑問,就是各國機器不分晝夜在解碼的這幾位細胞來源者,不管是政府單位宣稱有大於50 位以上的捐贈者或是賽雷拉(Celera Genomics)公司的21位捐贈者,真的就可以代表全人類嗎?他們是否帶有隱性疾病?因此,再回到現在的蛋白質體部分,是否也會出現研究對象及實驗設計的差異所導致的蛋白質表現差異?甚至一個小小的生理現象,如血液流體力在血管分岔處造成的蛋白質表現就不盡相同,或是癌症研究上,不管是細胞材料或手術檢體,可能皆已經是相當後期的生理表觀現象。......【更多內容請閱讀科學月刊第587期】