- 科技報導
文章專區
2023-04-18阿茲海默症不再無藥可治?新藥Lecanemab的機制與展望
496 期
Author 作者
陳韻如/中央研究院基因體研究中心研究員。
在臺灣大於65歲的年長族群除了關切自己的身體健康之外,更害怕罹患失智症(dementia)。一旦得到失智症,將使自己的人生經驗記憶全面崩壞,也會為照護者帶來生活上的諸多困難與不便。目前全世界的失智症患者已經高達4700萬人,但至今仍缺乏有效的治療藥物。失智症並不是單指一種特定的疾病,而是一群症狀的組合,其中阿茲海默症(Alzheimer's disease)在失智症的占比約為六成左右,且病人高達九成以上不屬於家族性遺傳,也就是說人人都有機會得到這個可怕的疾病。目前對於阿茲海默症有用的藥物並不多,但近期出現了一些變化。本文將介紹近期由美國食品藥物管理局(U.S. Food and Drug Administration,FDA)批准的新藥「Lecanemab」主要的機轉以及可能帶來的影響。
阿茲海默症的起點:Aβ蛋白胜肽聚集沉積
阿茲海默症的病理特徵為腦部出現錯誤摺疊的蛋白質堆積。患者大腦中有兩種主要的蛋白質堆積,其中一種為乙型類澱粉蛋白胜肽(amyloid-β,以下簡稱Aβ蛋白胜肽)堆積形成老年斑塊(senile plaques),另一種為tau蛋白堆積造成神經糾結(neurofibrillary tangles)。目前的學理為類澱粉蛋白假說(amyloid cascade hypothesis),認為Aβ蛋白胜肽早在患者發病的前20年就已開始累積,並且可以被影像探針偵測到。而後續隨著tau蛋白堆積、神經細胞逐漸死亡,特定腦區漸萎縮才開始發病。直到病人感受到記憶困難之前,許多病癥早已經在腦部形成。由於神經細胞無法再生,神經細胞的大片死亡便成為不可逆的病況。
Aβ蛋白胜肽是一種無結構的短鏈胜肽,主要由40∼42個胺基酸組成。在堆積的過程中會聚集形成有毒的多倍體聚合物──寡聚體(oligomer),成為原型纖維(protofibrils),進而形成長直鏈的不可水溶的成熟纖維(mature fibrils),長期下來便沉積在腦中形成老年斑塊(圖一)。
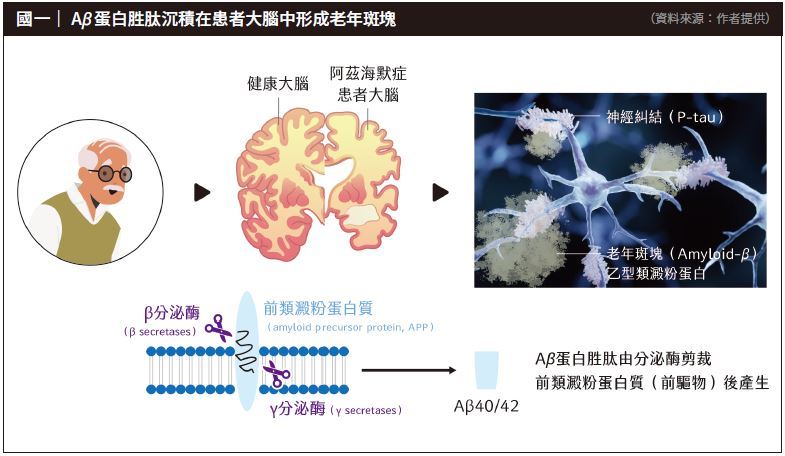
另外,許多家族性遺傳的阿茲海默症屬於早發型阿茲海默症,正是在Aβ蛋白胜肽序列上或是鄰近序列位置發現點突變,導致Aβ蛋白胜肽產出的量更多或是堆積的速率更為快速。多年來的研究指出,Aβ蛋白胜肽在阿茲海默症中像是手槍的板機,而tau蛋白像是子彈,要先有Aβ蛋白胜肽的刺激才會啟動下游tau蛋白的反應,進一步造成後續的腦部病變。所以Aβ蛋白胜肽長期被視為阿茲海默症病因的元兇,也是各大藥廠必爭的藥品標靶,本文的主角Lecanemab正是其中之一。
然而自Aβ蛋白胜肽發現以來,針對Aβ蛋白胜肽的藥物發展可說是屢戰屢敗,當中有小分子藥物抑制酵素剪出Aβ蛋白胜肽,也有Aβ蛋白胜肽疫苗。經過了30年的奮鬥,2021年FDA首次通過百健(Biogen)藥廠抗體藥物Aducanumab(商品名:Aduhelm)有條件地上市使用。此一抗體藥物主要針對Aβ蛋白胜肽組成的寡聚體,在臨床一期統計上出現顯著效用,後續便直接挺進臨床三期,雖然在腦影像探針的輔助下顯示病人腦部的老年斑塊清除效果十分顯著,但是對於他們的認知功能並沒有顯著改善。然而因為廣大的阿茲海默症病患皆面臨無藥可醫的情況,FDA還是讓Aducanumab上市,但仍持續要求百健進行臨床四期以追蹤藥物效果。由於病患的認知功能在藥物臨床三期的結果並未出現顯著改善,因此Aducanumab的效果也飽受質疑。這也使得類澱粉蛋白假說遭受質疑,而Aβ蛋白胜肽相關的研究也進一步成為箭靶,有些學者甚至懷疑它是否真的是造成阿茲海默症的原兇。
Lecanemab治療阿茲海默症的藥理機制
今(2023)年1月6日,FDA核准了本文主角Lecanemab(商品名:Leqembi)上市。Lecanemab由百健與日本衛采(Eisai)合作研發,是一種人源化的IgG1單株抗體,可以結合Aβ蛋白胜肽可溶性原纖維。它的第三期臨床試驗結果顯示,在使用Lecanemab治療阿茲海默症患者18個月後,患者認知下降的程度相較於安慰劑組減少了27%。這個消息也讓大家將阿茲海默症治療的焦點,重新放在錯誤折疊的Aβ蛋白胜肽上。
Lecanemab治療阿茲海默症的藥理機制與Aducanumab雷同,都是針對Aβ蛋白胜肽堆積物的抗體。目前認為這類抗體的藥理機制是以抗體辨識細胞外的Aβ蛋白胜肽堆積物後,腦中的免疫細胞再加以吞噬和清除。從藥廠提供的正子影像斷層掃描(positron emission tomography, PET)數據,也確實清楚地看到Aβ蛋白胜肽纖維在患者腦中被清除〔註〕。
〔註〕抗體是一種來自生物體內的蛋白質,具有針對其抗原的高親和力與專一性特性,因此占蛋白質藥物市場的最大宗,年產值超過1300 億美元。
Lecanemab和Aducanumab都是針對Aβ蛋白胜肽堆積物的抗體藥物,但是抗體藥物本身辨識目標的互補決定區(complementarity-determining regions, CDRs)序列不同,它們辨識的抗原序列(epitope)也可能不同,因此即便基本原理相同,還是會辨認到不同的堆積物並產生不同效果(圖二)。目前文獻指出兩種抗體都不會辨識Aβ蛋白胜肽單體,Lecanemab具高親和力可辨識原型纖維;而Aducanumab除了辨識寡聚體外,也會結合成熟纖維,可能因此造成兩者在藥效上的差異。
Lecanemab帶來的曙光與展望
對於日益惡化卻無藥可醫的阿茲海默症患者而言,找到一個真正有療效的藥物無疑是一項非常令人興奮的消息。Lecanemab的勝利也給了全球研究一劑強心針,不但確認了類澱粉蛋白假說,且真正在臨床上看到改變類澱粉蛋白對阿茲海默症的治療有效果。
然而,世界上藥物是沒有完美的,治療方法仍需要持續改進。由於Aβ蛋白胜肽堆積發生在病人出現失智症狀之前,如何找到潛在病人並提早開始用藥是一個問題。而目前Lecanemab的臨床試驗只針對輕微失智的阿茲海默症病患,尚未對於中重度阿茲海默症病患進行試驗,因此如何以Lecanemab治療中重度的病人也是一項挑戰。現階段Lecanemab改善失智程度的療效約為27%,對於改善失智程度上還有很大的進步空間。另外,Lecanemab的臨床試驗中有兩例患者因中風給予抗凝血劑或因心臟病而死亡。由於這些患者都患有腦澱粉樣血管病(cerebral amyloid angiopathy, CAA)〔註〕,可能因為Lecanemab治療後除了清除腦中的類澱粉蛋白,也移除了平時累積在血管壁上的類澱粉蛋白,反而引起血管出血。
〔註〕一種澱粉樣蛋白積聚在腦血管周圍的病症。
總結來說,阿茲海默症的病人數目隨著全球人口老化逐年增長,是不容忽視的問題。Lecanemab有機會在阿茲海默症發病早期阻擋一些連發的子彈,但阿茲海默症病程約為8∼20年,Aβ蛋白胜肽在Lecanemab介入前已造成的傷害,以及藥物未能阻擋的部分都是日後學術研究及藥物研發的重點。目前學界、藥界都還在持續研究阿茲海默症機制中的不同標的,例如tau蛋白的毒性與傳播,如何降低不良的發炎反應、增加堆積物清除的機制,或其他關鍵蛋白加成惡化影響,都是現今研究中如火如荼進行的目標。另外不僅是藥物本身的研發,阿茲海默症診斷工具的研發與診斷方法也是扶持藥物能找到適當病人用藥的關鍵。日後若能發展出不同標的的藥物,依病程及病人基因不同而依序或合併治療,將有機會發展出對他們最有效的治療方法。
延伸閱讀
1. Van Dyck, C. H. et al. (2023). Lecanemab in early Alzheimer's disease.New England Journal of Medicine, 388(1), 9-21.
2. Sevigny, J. et al. (2016). The antibody aducanumab reduces Aβ
plaques in Alzheime's disease. Nature, 537(7618), 50-56.
3. Couzin-Frankel, J., & Piller, C. (30 November 2022). As some hail new antibody treatment for Alzheimer’s, safety and benefit questions persist.Science. https://reurl.cc/pL9YQx