- 封面故事
- 2020年
- 604期-冠狀病毒的迫降(4月號)
文章專區
2020-04-01環狀包圍策略下的對抗—伊波拉疫苗
604 期
Author 作者
蔣維倫/泛科學PanSci專欄作家、故事專欄作家、udn 銘人堂專欄作家、前國衛院衛生福利政策研究學者。喜歡虎斑、橘子、白底虎斑和三花貓。
森林裡的死神-伊波拉
一歲半的男童正嘔吐著,高燒和血便等痛苦並沒有折磨他太久,2天後,男童死亡。沒有人預料到,屠戮上萬人的瘟疫即將開始。數日後的新年,神秘疾病蔓延。新年的第二週,曾照料男童的親屬、護理人員紛紛病發、快速死亡;接下來的一週內,更多人倒下,甚至參加男童喪禮的親屬也隨之死去。兩次的疫情調查將元兇指向霍亂,儘管無國界醫師組織加入調查,也未能辨識出死神的面目。
二月的第1天,一名男童的親屬前往該國首都,四天後在當地死亡;至此,死神已從一個僅31戶人家的小村落,踏進了都市;接下來長達兩年多的時間裡,死亡的氣息瀰漫整個西非,成千上萬人死去。
自1976年首次發現伊波拉出血熱(Ebola hemorrhagic fever, EHF)和病毒(Ebola Virus,圖一)後,它們的型態和致病機制引起科學家極大的好奇。目前推測自然宿主是森林裡的動物,如蝙蝠。人類則可能接觸罹病動物血液或體液,進而將病毒帶入體內。而人與人之間的傳染主要是透過:
● 接觸患者的血液或體液,如:嘔吐或排泄物等。
● 接觸被上述血液或體液汙染的物品。
因此患者的親屬或醫護人員等,就成了最危險的族群。病發時會突然高燒、嚴重倦怠、肌肉痛和頭痛等,接著嘔吐、腹瀉、腹痛、皮膚出疹與出血。嚴重甚至會肝受損、腎衰竭、中樞神經損傷、休克和多重器官衰竭,平均死亡率高達50%,部分疫情甚至超過90%的致死率。對於人類而言, 伊波拉幾乎就是死神,一個科學家頃盡心力想擊敗的死神。
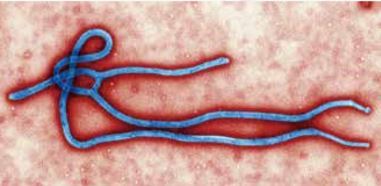
圖一:伊波拉病毒在穿透式電子顯微鏡(Transmission electron microscope, TEM)下的照片,再數位上色。(by CDC/Cynthia Goldsmith, Wikimedia)戴上伊波拉病毒的面具-疫苗的研發
面對如此棘手的傳染病,除了公衛策略外,其實,最有效的就是疫苗,讓人體擁有抵禦疾病的能力。在臺灣,醫院觸手可及、藥物取得快速且食物選擇多樣;相較於非洲,醫院稀缺,求診吃藥成本過高,而當地文化和肉食欠缺,禁止人民捕獵動物為食,恐是不切實際。因此透過研發疫苗,讓人們自身保有抵禦伊波拉病毒的能力,看來就是對抗病毒最好的選項之一。
而研發疫苗,是透過讓疫苗長得和病原體極其相似,使免疫細胞對此攻擊,製造出抗體。但是要如何讓病原體長得像伊波拉病毒呢?加拿大國家公共衛生部(Public Health Canada)採用「戴上伊波拉病毒的面具」策略,讓較無害的病毒,表面產出伊波拉病毒的醣蛋白(glycoprotein, GP)。2003年,他們利用基因重組的技術,讓水泡口腔炎病毒(vesicular stomatitis virus, VSV)戴上伊波拉病毒的面具。
水泡口腔炎病毒,是一種有著子彈般外型和脂質外膜的單股負鏈RNA(nonsegmented, negative stranded RNA)病毒,屬炮彈病毒科(Rhabdoviridae)。主要會引起馬、牛和豬等口腔發炎,雖然也會感染人類、引起類似感冒的表現,但不會出現水泡等嚴重的症狀。
科學家們剪下伊波拉病毒特定的醣蛋白基因,置換入水泡口腔炎病毒的基因組中,使成為表面帶有伊波拉病毒醣蛋白的水泡口腔炎病毒(rVSV-ZEBOV 或稱rVSV�GZEBOV-GP,圖二)。
伊波拉病毒生存週期與可能的傳播途徑
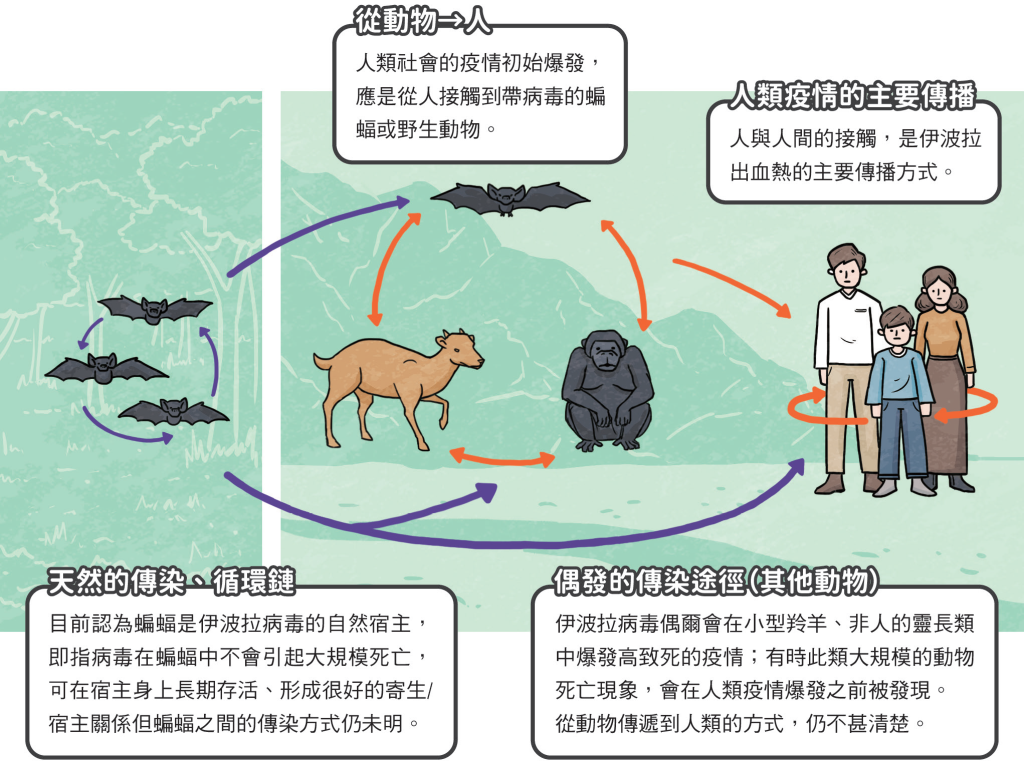 (許智翔繪製)
(許智翔繪製)
由於此重組病毒的基因不會鑲入人類細胞的DNA裡,因此具備安全性。加拿大公共衛生署開發成功後,將技術移轉到默克公司(Merck Sharp & Dohme, MSD),並更名為V920,持續進行大型動物與臨床試驗。2005年,首次在非人類靈長類動物進行試驗並有初步結果。
然而2014年,非洲爆發了大規模且恐怖的伊波拉疫情,瘟疫擴散六個國家,近三萬人感染、超過一萬人死亡;整體疫情延燒兩年半。此次疫情也震撼歐美各國,造成的恐慌和損失難以估計。而該疫情也折損了許多國家的醫護能力,利比亞約有8%醫護人員死於伊波拉,進而削弱了對其他疾病的對抗能力,如肺結核、麻疹和瘧疾等。
或許是西非2014年大規模伊波拉的爆發,加速了此疫苗的研發進度,人體試驗從2015年起快速進行,讓研發中的疫苗直接上了前線戰場,也成了此疫苗天然的臨床試驗場(右表)〔註二〕。也因此,科學家們需要一個完善的戰略,才能盡速地結束這場瘟疫。
真實世界裡,戰略物資該怎麼布署?
回到2014~2016年的瘟疫期間,每天都有成千上百人死去。若你是當時的公衛學家,手握這株效果未明的實驗疫苗,要採用什麼策略?才能同時達到「取得證據」和「拯救人命」的目的呢?
以下是伊波拉出血熱的特色:
● 人傳人的途徑以接觸傳染為主
● 潛伏期2~21 天
● 發病後才有傳染力
● 極高的致死率
在此嚴峻的條件下,當時的公衛團隊首次採取了「環狀包圍策略(randomized cluster (ring) vaccination design)」進行臨床試驗〔註三〕,力求同時達到「取得證據」和「拯救人命」的目的。
「環狀包圍策略」在消滅天花時取得極佳的成效,但在臨床試驗中仍未被嘗試。由於伊波拉為「接觸」傳染,因此科學家一聽到發病的消息,就風塵僕僕地趕往現場調查、分類,依「接觸的親密度」區分出風險,如圖三:
● 接觸患者的族群(Contacts),如:患者的家人、醫護人員、處理屍體的禮儀師或探病過的親友等,在試驗中稱作高風險者。
● 接觸「接觸患者族群」的族群(Contacts of Contacts),如:上述族群的親友、鄰居或同事等。
rVSV-ZEBOV機制和臨床試驗
環狀包圍策略
.png)
圖三:單人環狀包圍和多人環狀包圍策略。單人環狀包圍需要施打疫苗的對象包括感染者與第一層接觸感染者族群(紅藍圈內);從多人的環狀包圍來看,施打疫苗對象為最內圈的感染者和接觸患者的族群與第二圈的接觸「接觸感染者族群」的族群。
再依個人意願等因素,部分隨機「立即」接種疫苗;同時因此病致死率實在太高,為保障人權,剩餘的高風險者,3週後仍提供疫苗,屬「延遲」接種疫苗組。而在這次幾內亞採用的「環狀包圍策略」的三期臨床試驗結果顯示,「立即」接種疫苗的高風險者裡,2108 人在10~31天內皆無生病;而1429個「延遲」接種疫苗的高風險者裡,出現10名伊波拉出血熱患者。由於臨床試驗的效果出色,因此科學家也在試驗中期立刻停止「延遲」接種疫苗組,改採全面的「立即」接種疫苗。
rVSV-ZEBOV在西非戰場上挺過考驗,在疫苗設計和施打戰略上取得勝利,是基礎學術和公衛學者們通力合作的成功,也促使歐盟和美國在極短時間內完成審查〔註四〕,推出人類史上第一支伊波拉病毒疫苗——Ervebo。
臺灣該學到什麼?
Ervebo的出世並非一蹴可即,雖未達到完美,如免疫力能保持多少年、會不會有其他副作用等問題尚未了解,但已達到保護醫護人員,藉此提高醫護信心;在爆發時也能有效圍堵疫情並降低擴散。對於政府衛生部門而言,也能對疫情和相關研究更樂觀,並做出更適切的判斷。雖然因為西非的文化、交通和風俗民情等都和臺灣社會有著很大的差距,所以Ervebo 疫苗的成功或許無法完全複製到臺灣。但從設計與策略上仍可了解到一些重點:
● 完整的疫情調查能幫助策略的制定
● 民眾的信任能協助公衛策略推動、保障醫護人員安全
●「環狀包圍」在對抗特定傳染途徑疾病是事半功倍的策略
儘管臺灣不太可能需要Ervebo疫苗,但這是許多跨領域的學者們合作,加上幾十年的接種經驗,所共同豎立的里程碑,值得人們向那些先輩們致敬。
〔註一〕伊波拉病毒不會透過蚊蟲、空氣傳播。
〔註二〕此表僅列出部分試驗,更多資訊請見延伸閱讀一。
〔註三〕疫苗的環狀包圍策略在70 年代、消滅天花時取得極好的效果。
〔註四〕由於是因應緊急狀態,歐盟和美國都在上市聲明中加註許多條件,例如此疫苗在人體內的有效年尚未知,對於年齡過小的幼兒、孕婦等特殊族群效果也尚未評估。
延伸閱讀
1. DonataMedaglini and Claire-AnneSiegrist, Immunomonitoring of human responses to the rVSV-ZEBOV Ebola vaccine, Current Opinion in Virology, Vol. 23: 88-94, 2017.
2. World Health Organization, Major milestone for WHO-supported Ebola vaccine, 2019/10/18.
3. Ana Maria Henao-Restrepo et al., Efficacy and effectiveness of an rVSV-vectored vaccine in preventing Ebola virus disease: final results from the Guinea ring vaccination, open-label, cluster-randomised trial (Ebola Ça Suffit!), The Lancet, Vol. 389(10068): 505–518, 2017.