- 科技報導
- 焦點話題
文章專區
2025-04-15減緩抗微生物藥物抗藥性的全球前瞻策略
520 期
Author 作者
陳秀熙/臺灣大學健康數據拓析統計研究所教授
在去(2024)年的聯合國大會召開的抗生素抗藥性高階會議(UN General Assembly High-Level Meeting on antimicrobial resistance 2024)上,抗生素抗藥性(antimicrobial resistance, AMR)再次成為重要討論議題之一。各國元首和政府代表一致通過了一系列聲明,強調需立即採取行動以保護我們治療感染的能力,試圖喚起各國對抗藥性問題的關注。除了強調感染預防、疫苗接種和減少抗生素的不當使用外,對新型抗生素和治療方法的研究也至關重要。因此系列聲明內容包括改善感染預防的具體目標、籌措資金的計畫,以及承諾提供一億美元的資金,以支持在2030年前讓至少60%的國家擁有資金充足的AMR國家行動計畫。
為因應對抗AMR的號召,世界衛生組織(World Health Organization, WHO)最近也制定了全球行動計畫,呼籲地方、國家及全球利益相關者和監管機構採取多方面且協調一致的行動。最終目標是減少或防止AMR的發展,降低對人類和動物健康的威脅以及全球經濟的影響,並延長現有治療方法的使用壽命。
根據WHO的行動計畫,包括中國(全球抗生素主要消費國之一)在內的178個國家已制定了遏制AMR的國家行動計畫。然而,目前僅有約25%的國家有效落實了這些計畫。遏制AMR需要全球協作、政策支持及技術創新。透過加強疫苗接種、提高抗生素可及性、強化感染控制、推廣診斷技術及改進監測數據等行動加以整合,才可能有效減少AMR對健康與經濟的威脅。
抗生素抗藥性防治基石
感染預防與控制計畫,是應對AMR的基石,尤其在中低所得國家(lowand middle-income countries, LMIC)更是如此。最新分析估計,若能確保水資源、衛生設施及疫苗接種普及,每年可直接預防超過33.7萬起與AMR相關的死亡,還能減少抗生素的消耗,進一步降低耐藥性感染。
疫苗對AMR的影響,則包括了直接與間接的效益。例如,藉由疫苗預防細菌感染,可減少對第一線和第二線抗生素的需求,降低耐藥性菌株的產生以及住院人數,這也有助於避免AMR從社區向醫院擴散。確保足夠的疫苗接種覆蓋率以實現群體免疫,則可有效阻止耐藥菌株的傳播,例如肺炎鏈球菌(Streptococcus pneumoniae)結合型疫苗和流感嗜血桿菌(Haemophilus influenzae)疫苗的應用。抗病毒疫苗則能降低病毒性疾病的發生率,減少因病毒感染而不當使用抗生素的情況,幅度達13∼64%。與抗生素耐藥性相比,疫苗耐藥性相對罕見,因為疫苗通常在感染發生前預防微生物的生長,減少了AMR的發展風險。
提高有效抗生素的可及性,特別是在中低所得國家,將會是實現2030年「10-20-30全球目標」的關鍵步驟〔註1〕。其中最重要的措施為「廣泛使用-謹慎使用-保留使用(Access-Watch-Reserve)框架」〔註2〕,措施包括降低抗生素研發成本、提高專利到期抗生素的仿製藥可用性〔註3〕、加速抗生素可及性及政策激勵新抗生素的開發。
〔註1〕也就是AMR 相關死亡減少10%、人類中不適當抗生素使用減少20%、動物中不適當抗生素使用減少30%。
〔註2〕廣泛使用抗生素是指廣泛可及且抗藥性風險低的窄譜抗生素;謹慎使用抗生素用於治療更嚴重的感染;保留使用抗生素則作為治療多重耐藥感染的最後手段。
〔註3〕例如由WHO 設立的加速全球抗生素可及性公平分配SECURE(Securing Acess to Effective Antibiotics)平臺,是一項由 WHO 推動的全球倡議,目標為加速抗生素的可及性與公平分配,協助國家選擇、採購、分發與使用具成本效益且適應當地抗藥性趨勢的抗生素,推動合適層級抗生素的使用。
研究顯示,現階段全球社區藥房中非處方抗生素的發放比例高達63.4%,而且在2003年至2023年間無顯著改善。主要原因包括患者對抗生素的強烈需求與知識缺乏、醫療服務可及性差或成本高、販賣抗生素具經濟誘因、抗微生物管理薄弱。針對這些問題,需採取措施提升患者與處方者的教育和意識,加強醫患溝通,並在社區和醫院中強化抗微生物管理。
加強微生物抗藥性的監測與診斷
2015年,WHO啟動了全球抗微生物抗藥性與使用監測系統,這是第一個標準化AMR監測的全球協作計畫。截至目前,已有127個地區參與。儘管全球監測點從2017年的729個增加至2021年的2萬4803個,但監測數據仍不完整,特別是在開發中國家。數據異質性是現有AMR監測系統的一大挑戰,阻礙了疾病盛行率、抗生素使用與病原體基因型之間的有效比較與解釋。此外動物AMR監測系統的缺乏也是一個重要問題,原因包括資源限制、法律框架缺失以及動物AMR數據不足。
除了監測之外,診斷技術的創新也非常重要,準確診斷對於減少抗生素的誤用或過度使用至關重要。感染診斷的不確定性,常導致醫師開列不必要的抗生素。高通量分子診斷技術(high-throughput molecular diagnostics),例如全基因組定序(whole genome sequencing, WGS),在過去十年間逐漸用於快速的微生物檢測、AMR監測及疫情調查。全基因組定序可提供病原體能力或特徵的最高分辨率,有助於快速預抗微生物敏感性及揭示傳播路徑。然而,這種技術需要大量基礎設施、專業知識和投資,因此在AMR盛行的中低所得國家應用有限。
新興的非抗生素抗微生物治療
2022年,WHO報告顯示,臨床藥物開發管線中有80種新型抗微生物藥物,包括46種傳統藥物和34種非傳統藥物。其中34種藥物處於第一期臨床試驗,29種處於第二期臨床試驗,14種處於第三期臨床試驗,3種正在接受監管評估。46種傳統抗生素中更有28種(61%)針對WHO優先關注的病原體進行研發。對抗微生物的療法並不止於抗生素,現階段更有抗體、抗體-抗生素偶聯物(antibody-drug conjugates, ADCs)、抗微生物肽(antimicrobial peptides, AMPs)、噬菌體(phages)、基因治療及各種聯合療法發展中,以下逐一列舉:
1. 抗體:現階段人類單株抗體(monoclonal antibody, mAb)主要用於治療癌症和自體免疫疾病,在近期也成功用於治療新冠併發重症(COVID-19)。Palivizumab是首個顯示對感染性疾病有效的人類單株抗體,1998年由美國食品藥物管理局(Food and Drug Administration, FDA)批准,用於預防高風險嬰兒的呼吸道融合病毒(respiratory syncytial virus, RSV)感染。隨後,2016年Obiltoxaximab獲准與抗生素聯用,應用於治療吸入性炭疽(inhalation anthrax)。這些發展凸顯了人類單株抗體在抗微生物治療的潛力。
2. 抗體-抗生素偶聯物:抗體-抗生素偶聯物概念上源自於抗體藥物偶聯物,是由單株抗體和強效抗生素共價結合而成的先進藥物。抗體-抗生素偶聯物的設計旨在選擇性地結合特定抗原,並將抗生素直接送達感染部位。因此,抗體-抗生素偶聯物最終有望用於應對結核病(tuberculosis)和其他具有挑戰性的感染。理論上,透過高度特異性的抗體瞄準病原體(pathogen-targeting antibodies),可以將廣譜抗生素轉變為病原特異性或部位特異性的抗生素,將廣譜抗生素的副作用最小化,並減少對共生菌的無差別殺傷。
3. 抗微生物肽:抗微生物肽和抗生物膜肽是天然宿主防禦肽的一部分,通常是小型(小於50個胺基酸)、帶正電的親水性分子。它們有強大且迅速的廣譜抗微生物活性,即使對多重耐藥的新興抗藥菌群ESKAPEE〔註〕病原體也有效,因此抗微生物肽在應對抗藥性方面應擁有巨大的潛力,誘發抗藥性的風險極低,且一些抗生物膜肽對生物膜具備優異的廣譜活性,對於生物膜相關感染治療效益可達65%。
〔註〕分別為糞腸球菌(Enterococcus faecalis)、金黃色葡萄球菌( Staphylococcus aureus )、肺炎克雷伯氏菌(Klebsiella pneumoniae)、鮑氏不動桿菌( Acinetobacter baumannii )、綠膿桿菌(Pseudomonas aeruginosa)、腸桿菌屬(Enterobacter)及大腸桿菌(Escherichia coli )。
4. 抗微生物肽-抗生素聯合療法:抗微生物肽與抗生素聯合療法是另一個具有吸引力的策略,可以增強整體抗微生物活性,並減少抗微生物肽和抗生素的劑量依賴性毒性。隨著肽模擬技術、人工智慧(artificial intelligence, AI)輔助肽設計以及先進奈米顆粒、水凝膠、基於DNA或RNA的藥物傳遞系統興起,對於抗微生物肽的研究越來越多,旨在提高療效、安全性和穩定性。
5. 噬菌體:噬菌體是能夠感染細菌的病毒,在生物圈中極為豐富。儘管它們在1915年就被發現,噬菌體的潛在治療意義卻一度被抗生素的發展所掩蓋。隨著抗藥性微生物的崛起,噬菌體作為抗生素替代品的可能性重新引起關注。雖然噬菌體抗性已經為人所知,但噬菌體在對抗抗藥性方面還有許多潛在優勢。噬菌體在治療由多重耐藥ESKAPEE病原體引起的肺炎、敗血症、腦膜炎、傷口感染和角膜感染等疾病中有很大的潛力。在約87%的研究中均顯示可根除細菌,具有良好的耐受性和安全性,副作用僅7%,且通常在停止治療後自行消退。儘管有潛力,然而到目前為止,基於噬菌體的治療尚未在隨機對照試驗中獲得充分臨床驗證,因此目前的臨床運用僅限於醫學倫理宣言《赫爾辛基宣言》(Declaration of Helsinki)第37條所述的範圍,也就是在缺乏有效療法且病患知情同意的前提下,才能夠採行。
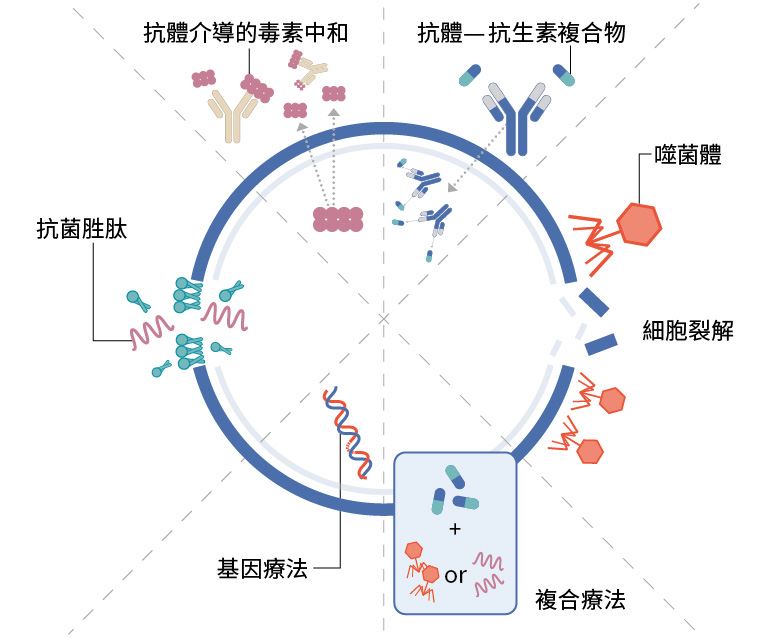
圖片來源:Ho, C. S. et al., 2025.6. 基因治療:利用CRISPR/Cas9基因編輯技術〔註〕重新編程Cas9核酸酶,能在細菌中引入不可逆的染色體損傷,使細胞死亡。這項發現讓Cas9核酸酶有機會促進序列特異性抗微生物製劑,可以選擇性地殺死一種或多種特定的細菌。臨床前研究結果顯示,利用CRISPR基因編輯技術,將能摧毀抗生素抗藥性強、致病性強的金黃色葡萄球菌(Staphylococcus aureus)。這項策略有可能可以做到選擇性殺菌,不會干擾其他非致病性的微生物群。由於Cas9核酸酶的抗微生物能力已被確立,CRISPR/Cas9被視為小分子抗生素的有力替代品。然而仍需進一步研究來改進傳遞方法、純度、可擴展性和宿主範圍,以促使基因治療的廣泛應用。
〔註〕細菌使用多種機制來抵抗噬菌體,包括CRISPR免疫系統。CRISPR 的發現促使了各種新型基因技術的發展,尤其是使用CRISPR/Cas9 核酸酶系統進行基因組編輯。
新興AI技術協助破解微生物藥物抗性難題
隨著AI技術的進步、計算能力和資源的提升,以及包括電子健康紀錄和組學(omics)〔註〕數據在內的大數據可用性,AI正逐漸成為應對傳染病和解決AMR的強大工具,應用範圍涵蓋抗生素敏感性測試、AMR監測、抗微生物管理、診斷以及抗微生物藥物的研發。
〔註〕指生物學中對各類研究對象(一般為生物分子) 的集合所進行的系統性研究, 例如基因體學(genomics)、轉錄體學(transcriptomics)、蛋白質體學(proteomics)等。
傳統的抗生素敏感性測試依賴細菌作為生長指標,通常需要24∼48小時,而如結核分枝桿菌(Mycobacterium tuberculosis)等生長緩慢的細菌可能需要更長時間,因此耽誤了使用了抗生素治療的最佳時間點。機器學習愈來愈常用於分析全基因組定序數據,以實現快速的抗生素敏感性預測和AMR監測,減少了全基因組定序分析所需的大量生物資訊資源或專業知識。這種方法在大規模AMR監測計畫中展現了巨大潛力,特別是在中低所得國家。
其中一種頗富潛力、由機器學習驅動的奈米運動平臺可以透過測量細菌振動,在2∼4小時內快速完成無需依賴細菌生長的敏感性測試,準確性高達90∼99%。基於電子健康紀錄數據的抗生素敏感性高精確度機器學習模型已成功開發,可用於指導特定且窄譜的抗生素使用,與臨床醫師的處方治療相比,能有效減少約70%的二線抗生素使用以及約20%的不適當抗生素使用,促進抗微生物管理。此外,深度學習可以實現基於影像的自動化及快速化醫學診斷,目前已應用於多種傳染病的診斷,例如結核病和感染性角膜炎。
由全球生態星球健康的角度對應抗藥性議題
導致抗藥性和抗生素失敗的因素包括抗生素的廣泛使用、替代療法的稀缺、社會經濟環境、醫療和農業實踐、旅遊以及全球化。解決抗藥性問題需要持續且協作的努力,這包括當地和國際政策的改善、抗生素使用的教育、加強監測系統、防止與抗藥性相關的感染和傳播,並開發新技術和替代抗菌療法。必須促進協作和可持續的研究努力,而且要從人類、動物及生態環境的全方位星球健康視野出發。
AMR是「健康一體」(One Health)〔註〕的問題,在去年的聯合國大會上再次強調,必須藉由減少抗生素汙染及控制抗藥性基因在環境中的傳播來遏制抗藥性問題。現階段,具抗藥性的菌種會透過人類、家養及野生動物、水與空氣等環境相互傳播;水、衛生與衛生設施(water, sanitation and hygiene, WASH)等公共設施的不足、可負擔醫療服務以及適當抗生素的缺乏,則會進一步加速AMR的傳播。AMR已成為一場緊迫的公共健康危機,並且是一個需要在人類、農業和環境部門間協作的「健康一體」優先事項。健康一體的推動需要多部門合作,成功推動計畫仰賴所有利益相關者的共同努力。WHO、聯合國糧食及農業組織(Food and Agriculture Organization of the United Nations, FAO)以及世界動物衛生組織(World Organisation for Animal Health, WOAH)正密切合作,確保各部門能夠採取有效行動,減少AMR風險。
〔註〕將人類健康、動物健康及環境保護納入統一的政策框架中。
愈來愈多的研究將AMR相關的注意力從人類因素轉向動物因素,因為來源於動物的AMR問題更加嚴重。早期研究指出,全球73%的抗生素使用在農場動物,主要用於食品生產。如果這個趨勢得不到控制,可能會成為嚴重問題。目前許多國家會透過收取使用費和設定動物用抗微生物藥物的使用上限,來減少這些藥物的用量。此外,農業部門也主動參與,確保動物藥物的負責任使用,並開發各種抗微生物管理計畫。例如英國「農業藥品負責任使用聯盟」(Responsible Use of Medicines in Agriculture Alliance, RUMA)鼓勵創新和積極努力,改善動物藥品的負責任使用,同時確保最佳的動物健康和福祉。未來應該進一步制定關於動物用抗微生物藥物的指導方針,以應對藥物使用可能帶來的風險。這些資訊不應局限於提供人類使用的抗微生物藥物,而是要提高人們對整體AMR現狀的意識。
在中低所得國家推行「健康一體」應對AMR面臨的挑戰,比在高所得國家(high-income countries)更多,因為中低所得國家受到貧窮、腐敗和醫療系統問題的影響,例如清潔用水缺乏、衛生問題以及抗微生物藥物的可及性,使環境本身就容易引發疾病。此外,一項研究指出,中低所得國家的農業部門也面臨更多問題,由於缺乏專業獸醫和支持系統,農民在面對動物細菌感染時只能依賴抗生素。然而,儘管許多高抗性細菌菌株主要是在這些國家傳播,AMR監測仍大多實施於高所得國家。這反映了醫療系統和AMR法規方面的發展差距亟需解決。中低所得國家也許可以透過引入抗微生物敏感干預措施來加強「健康一體」,例如改善清潔用水的可及性。此類措施對於資源有限的中低所得國家來說,更具成本效益且可持續性強。
強化國際合作,制定標準並投資研發
聯合國大會呼籲制定國際通用的抗生素使用準則,特別是在動物養殖業及農業領域。過去幾十年中,抗生素在工業化養殖的廣泛應用被認為是抗藥性加速擴散的原因之一。聯合國希望通過國際協議,促進無抗生素農業技術的推廣。
AMR的影響不分國家,遍及所有年齡層,但受影響最鉅的仍屬中低所得國家,以及處於弱勢環境的人群。此外,AMR的發展和擴散也明顯發生在環境中,例如水道、牲畜和食品生產領域。應對AMR需要全球性的解決方案和夥伴關係,以及公共與私人組織之間的多部門合作,方能推動創新和進步。呼吸和重症監護領域的專業人士在對抗AMR中處於核心位置,既要在保護現有抗生素資源方面發揮關鍵作用,也要積極推動對新療法的研究。聯合國祕書長在大會中指出,抗藥性問題不僅是一國或地區的挑戰,更是全球共同面臨的公共健康危機。他強調應加速建立全球性合作平臺,包括資源共享、數據交換及跨國研究計畫,特別是在中低所得國家和地區進行建設。聯合國提出了「全球抗藥性應對基金」,目標在未來五年內籌集100億美元,用於抗藥性相關的研究、教育及監測。
WHO於2015年啟動AMR全球行動計畫(Global Action Plan on AMR, GAP-AMR),主要目標是提高抗微生物藥物在人體和動物健康中的使用效能,這需要建立良好的監管系統。各國的藥品監管單位不同,預期會制定各自的AMR國家行動計畫,因地制宜達到全球行動計畫的總體目標。根據WHO的報告,目前已有18個國家和地區建立了多方參與的AMR國家行動計畫,另有6個國家正在完成最後階段的國家行動計畫制定工作。
另一項計畫是全球抗微生物藥物抗性與使用監測系統。此計畫目的是推動全球範圍內對抗微生物藥物抗性的監測,並找出抗微生物藥物抗性產生的原因。這項計畫還將提供建議與指導,協助各國在必要時採取補救措施。聯合國大會最終呼籲,各國應在2030年前制定和實施符合全球抗藥性行動計畫的國家策略,並定期向聯合國報告進展情況。
全球抗藥性研究的資金長期不足,聯合國強調應加大對新型抗生素、疫苗及替代療法的研發投入。此外,針對目前抗生素市場利潤低的問題,聯合國提倡建立「市場激勵機制」,吸引更多企業參與研發。若能與鄰近國家共同參與亞太區域抗藥性合作計畫,也將提升區域治理能力。
共同對抗抗生素抗藥性的「隱形大流行」
抗生素抗藥性是一場緩慢但致命的「隱形大流行」,影響著全球的健康安全與經濟穩定。面對這一挑戰,各國亟需採取更加嚴格的政策措施,並促進創新研發和全民教育。臺灣在抗藥性治理方面已取得顯著成效,但未來仍需持續加強與國際合作,推進「健康一體」框架的落實,從根本上解決抗藥性帶來的危機。
延伸閱讀
Ho, C. S. et al. (2025) Antimicrobial resistance: a concise update. The Lancet 6(1).