- 封面故事
- 2025年
- 664期 - 實驗動物的過去與未來(4月號)
文章專區
2025-04-01臺灣科學家如何打造沒有動物實驗的未來?方圓細胞生醫、久浪智醫團隊專訪
664 期
Author 作者
撰稿採訪|羅億庭 生醫系畢業的打工仔,喜歡冷知識、諧音梗,還有很圓的貓。
Take Home Message
• AI 技術的發展使得藥物研發可以先透過模擬蛋白質結構提升藥物精準度,再搭配3D 細胞培養與器官晶片,驗證藥物在生物體上的效力。
• 傳統的3D 細胞培養方法可能出現細胞增殖不均勻、難以標準化、細胞回收困難等問題。臺灣方圓細胞生醫團隊開發R3CE® 技術,讓細胞自然且均勻地增生為球狀,更能夠擴增體內少量的罕見細胞。此技術成功地克服了傳統方法面臨的難題。
• 久浪智醫團隊開發技術門檻高的肺部器官晶片,在體外打造出類似體內運作的環境,可用於吸入性藥物測試、病毒感染研究、空氣汙染研究等。
讀者在購買化妝品、保養品時,是否曾留意過有些產品包裝上會出現一隻「跳躍兔子」(Leaping Bunny)的標章呢?此標章由國際零殘忍組織(Cruelty Free International )與化妝品消費者資訊聯盟(Coalition for Consumer Information in Cosmetics, CCIC )共同推動,獲得認證的產品從原料供應鏈到開發、生產的整個過程中皆不得進行動物試驗,並需接受定期審查。這項跳躍兔子計畫,希望透過標章認證,推廣無動物試驗的理念以及動物試驗的替代方案,至今已有多家化妝品和保養品品牌獲得此標章,例如LUSH、The Body Shop 等。
回顧過去,早在西元前就已有古希臘哲學家嘗試解剖動物,研究生物的構造和生理機能,進而推演人體生理結構與功能,各種動物試驗也對現代醫學發展具有深遠的影響。但為什麼到了21 世紀,人們反而開始呼籲取消動物試驗,並積極尋找動物試驗的替代方案?首先,倫理與動物權意識的提升讓愈來愈多人認為不該為了人類需求而犧牲動物,歐盟(European Union, EU)也在2013 年全面禁止使用動物測試化妝品;美國食品藥物管理局(Food and Drug Administration, FDA )則在2022 年批准了《FDA 現代化法案2.0 》(FDA Modernization Act 2.0, FDAMA 2.0),不再強制規範新藥開發時必須實施動物試驗,期望減少研究人員對動物試驗的依賴,並推動替代技術發展,也藉此縮短藥物開發的時間。此外,也有研究顯示,許多動物試驗的結果無法直接套用到人類身上,例如某些癌症新藥在小鼠試驗中有效,但到了人體臨床試驗階段,藥物的成功率卻不到5%。在種種因素的推動下,科學界開始尋找更精確的測試方法來取代動物試驗。
而在臺灣,也有一群科學家正搭著這股浪潮,致力於動物試驗的革新。

受訪|陳冠宇
久浪智醫的創辦人,帶領公司開發新一代器官晶片與AI 驅動的生醫分析平臺,並與全球藥廠及醫療機構合作,以「NoAnimal, No Human, Just Technology」為目標,推動精準醫療與實驗自動化。(作者提供)
受訪|張瑛芝
為方圓細胞生醫的創辦人暨執行長,以領先業界的前瞻技術,開創3D 細胞培養與循環腫瘤細胞研究的新局面。獨創的R³CE® 技術,能在短短兩週內將單一稀有細胞培育成三維立體模型,實現「1 Cell, 2 Weeks, 3D Models to save lives」的願景,為精準醫療與再生醫學帶來劃時代的突破。(李珈萍拍攝)
臺灣的動物替代試驗發展
新藥開發是一段複雜而漫長的過程,從早期的藥物設計到實驗驗證,每一步都影響著最終的成功率。
在過去,研究人員需要透過大量動物實驗來篩選可能有效的化合物,但近年來人工智慧(artificial intelligence, AI)的模擬技術正改變這一切。像是由DeepMind 開發出的AlphaFold(圖一),就能夠預測蛋白質結構,大幅提升藥物設計的精準度,讓研究人員在進入實驗階段前能更快找出潛在有效的藥物。然而透過AI 模擬出的藥物,仍需要在生物環境中驗證,才能確保它的效果。這時候3D 細胞培養與器官晶片等技術就成為關鍵,它們讓科學家能在體外模擬人體組織、進行藥物測試,無需依賴傳統的動物實驗。而這也是許多臺灣團隊正在努力的方向――建立一個能夠取代動物試驗的完整生醫技術平臺。
圖一 | AlphaFold 頁面。(Adobe Stock)
3D 細胞培養
方圓細胞生醫創辦人暨執行長,同時也是美國史丹佛大學(Stanford University)化學工程學系兼任教授的張瑛芝,就與我們分享了團隊建立3D 細胞培養的過程。張瑛芝團隊自2000 年開始研究3D 細胞培養,當時基因定序剛開始發展,而人類基因體計畫(Human Genome Project, HGP)的定序也在2003 年完成。這些進展促使學界開始思考――如果可以直接在人類細胞上做實驗,那我們為什麼還要依賴動物?於此同時,幹細胞研究、奈米科技等領域也逐漸有所突破,種種技術的交會讓研究人員有了發展3D 細胞培養的可能性。但3D 細胞培養的優勢在哪裡?它跟2D細胞又有什麼區別(圖二)?
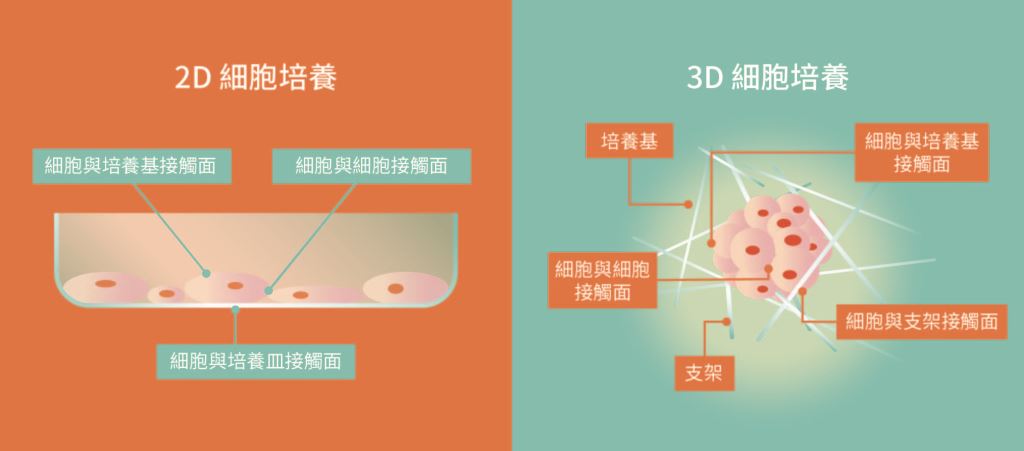
圖二
由於人體內的細胞並非單獨存在,而是與周圍細胞、組織形成複雜的互動關係,因此3D 細胞培養可以比傳統的2D 單層培養更真實地模擬細胞生理環境,使細胞的行為更接近它在人體內的狀態。這種技術對於藥物開發、疾病研究,以及器官再生等領域的研究具有重要價值。不過要創造一個適合3D 細胞生長的環境可不是件容易的事,過往主要的3D 細胞培養方法可分為三種:
1. 生物反應器( bioreactor):在受控的環境中持續攪拌,讓細胞懸浮於培養液,促使它們聚集成球狀結構。但缺點是可能會有細胞分布不均勻,容易形成大小不同的細胞團,而影響實驗結果。
2. 支架培養( scaffold-based ):利用具有生物相容性的水膠作為支架,讓細胞生長在水膠中,有如果凍裡的椰果般,於水膠中增殖並形成3D結構。不過此種作法在取出細胞時較困難,且不利於影像觀察。
3. 無支架培養(scaffold-free):改變培養皿表面的塗層,使細胞無法完全貼附於容器表面,讓細胞四處移動、彼此聚集成球。但也導致細胞結構不穩定,難以標準化。……【更多內容請閱讀科學月刊第664期】